面包屑
核梭杆菌感染牙龈上皮细胞导致NLRP3炎性小体依赖性分泌IL-1β和危险信号ASC和HMGB1
它的目的是解决什么问题?
牙周炎是世界上最常见的慢性疾病之一. 了解免疫系统如何识别引起牙周病的细菌有助于预防牙周病.
它是如何工作的??
研究人员用 F. nucleatum,然后用各种细胞和分子方法检测细胞随时间的反应. 他们发现这种感染引发了免疫系统的一连串反应. 更具体地说,F. 核体感染激活NF-κB(一种控制DNA转录的蛋白质复合体), 细胞因子的产生和细胞存活), 哪个会转移到细胞核, 刺激促炎基因的表达, 包括编码细胞因子蛋白IL-1β前体的基因, 或pro-IL-1β. 除了, 感染激活NLRP3炎性体, 进而激活半胱天冬酶-1, 导致成熟IL-1β的加工和释放. 危险信号ASC的释放进一步放大了炎症, 和HMGB1蛋白, 哪个与细胞核中的染色质结合.
现实世界的影响是什么?
在短期内, 研究人员对牙龈上皮细胞对细菌感染的复杂反应有了更深入的了解. 从长远来看, 也许牙周病可以通过靶向/增强口腔免疫反应来治疗.
下一步是什么?
这些研究是用培养的牙龈细胞系进行的. 其他基因调节炎症体本身的活性. 研究人员计划在口腔感染的动物模型中研究炎症小体和调节炎症小体的基因, 并研究这些基因在人类牙周病中的功能.
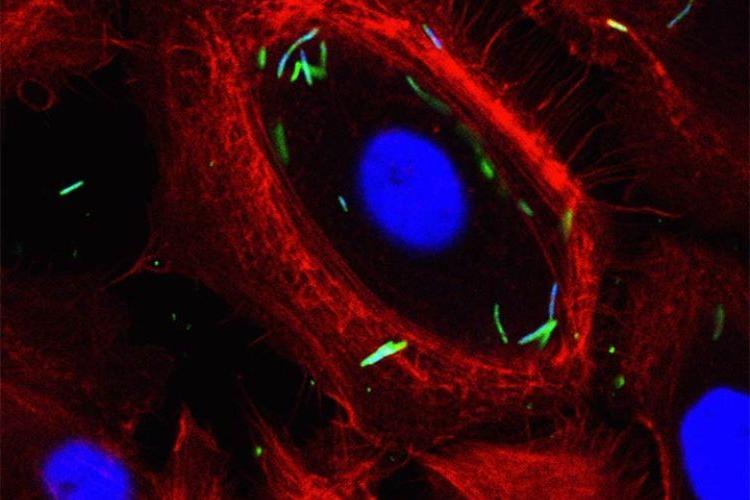
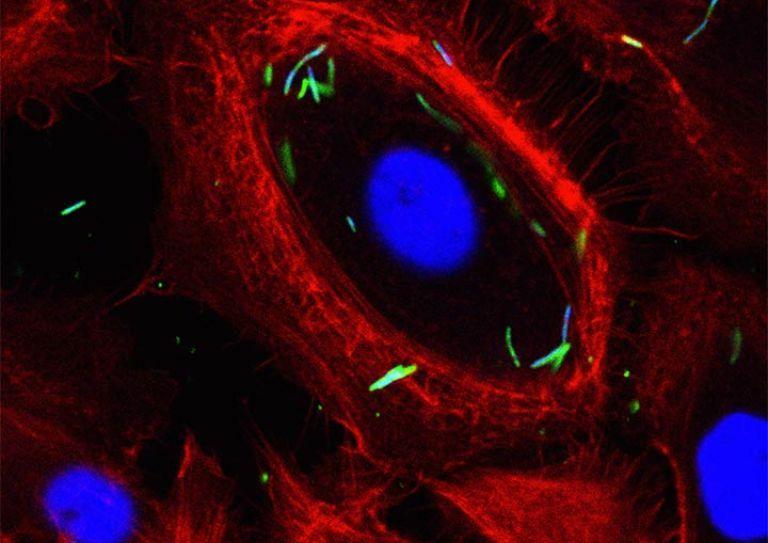
细胞内定位 梭菌属nucleatum 在通用电气. 免疫荧光共聚焦显微照片 F. nucleatum (MOI为100)1h. 通过宿主细胞中间的单一光学切片证实了细菌在细胞内的定位. 用phalloidin-tetramethylrhodamine B异硫氰酸酯(红色)对固定的gec进行染色,显示肌动蛋白细丝, 和反F. nucleatum 抗体(绿色). Bar代表20µm.
Source
核梭杆菌感染牙龈上皮细胞导致NLRP3炎性小体依赖性分泌IL-1β和危险信号ASC和HMGB1,第18卷,第7期,2016年7月,970-981页
作者
霏欧纳问. 中方通过
北京大学生物医学科学系
太平洋,亚瑟·杜戈尼牙科学院
拉里•约翰逊
北京大学生物医学科学系
太平洋,亚瑟·杜戈尼牙科学院
免疫生物学项目,Biofísica卡洛斯研究所
查加斯·菲尔霍,里约热内卢联邦大学
乔安·罗伯茨
牙周病与新发病原体科
佛罗里达大学盖恩斯维尔分校研究所
Shu-Chen挂,
北京大学生物医学科学系
太平洋,亚瑟·杜戈尼牙科学院
Jungnam李
牙周病与新发病原体科
佛罗里达大学盖恩斯维尔分校研究所
Kalina Rosenova Atanasova
牙周病与新发病原体科
佛罗里达大学盖恩斯维尔分校研究所
佩蓉黄
南京医科大学分子与临床免疫学研究中心
台湾广东大学
Ozlem Yilmaz
牙周病与新发病原体科
佛罗里达大学盖恩斯维尔分校研究所
大卫·米. Ojcius
北京大学生物医学科学系
太平洋,亚瑟·杜戈尼牙科学院